来源公众号:ExpCon医学科普
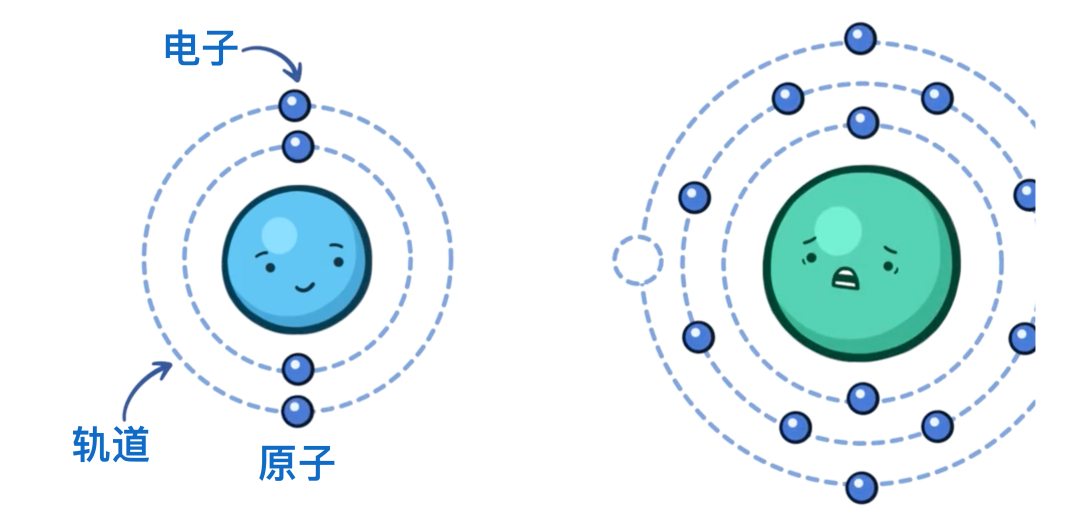
原子中的电子存在于称为“轨道”的空间中,每个轨道可容纳不同数量的电子对。
自由基是指外层轨道中仅含单个电子(即未配对电子)的分子。自由基会从周围的分子中夺取电子以使自身稳定,这种行为正是引发问题(如潜在细胞损伤)的根源。
当分子获得或失去电子时,便会形成自由基。在人体内,自由基既可通过生理途径(如正常代谢过程)产生,也可由病理途径(如疾病)引发。
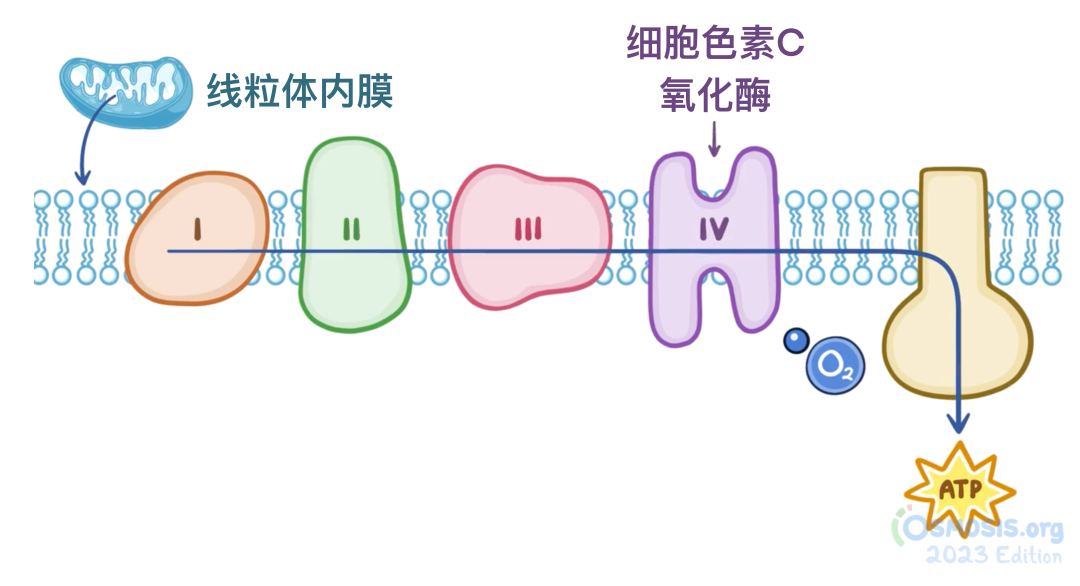
自由基的一个主要生理来源是细胞呼吸,也称为氧化磷酸化。氧化磷酸化是通过将电子传递至线粒体内膜中的蛋白复合体来生成ATP的过程。
这些复合体共同构成电子传递链,电子在其中逐级传递,最终到达氧分子,并形成用于合成ATP的质子梯度。该过程的最后一步由细胞色素C氧化酶(又称复合体IV)完成,它将电子转移给氧分子。
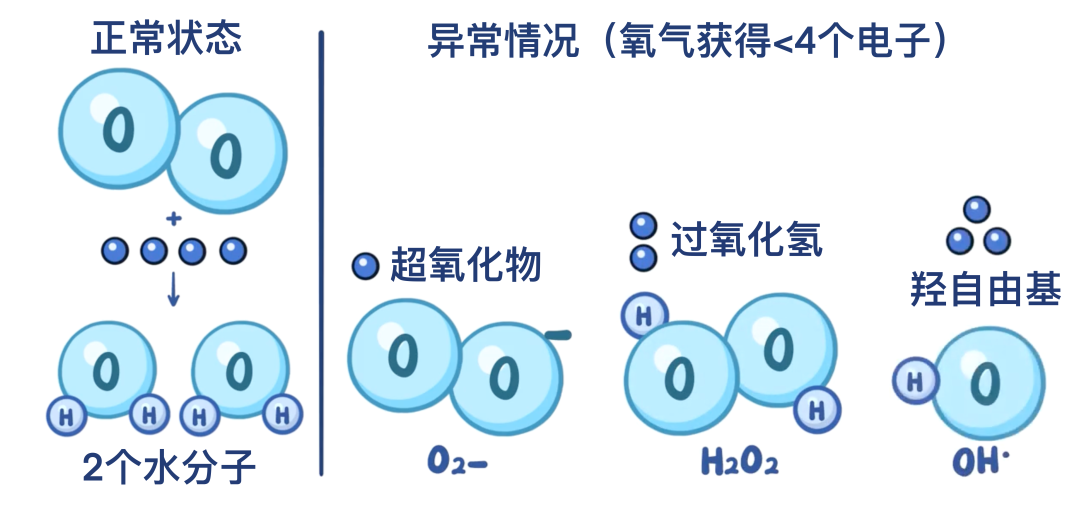
正常情况下,氧分子获得四个电子后会转化为水。然而,当氧分子未能获得全部四个电子时,其轨道中会出现未配对电子,从而形成自由基。由于这些自由基由氧分子形成,因此统称为活性氧簇(ROS)。
当氧分子获得一个电子时,会转变为超氧化物(O₂⁻);获得两个电子时成为过氧化氢(H₂O₂);获得三个电子时则形成羟自由基(OH·)。
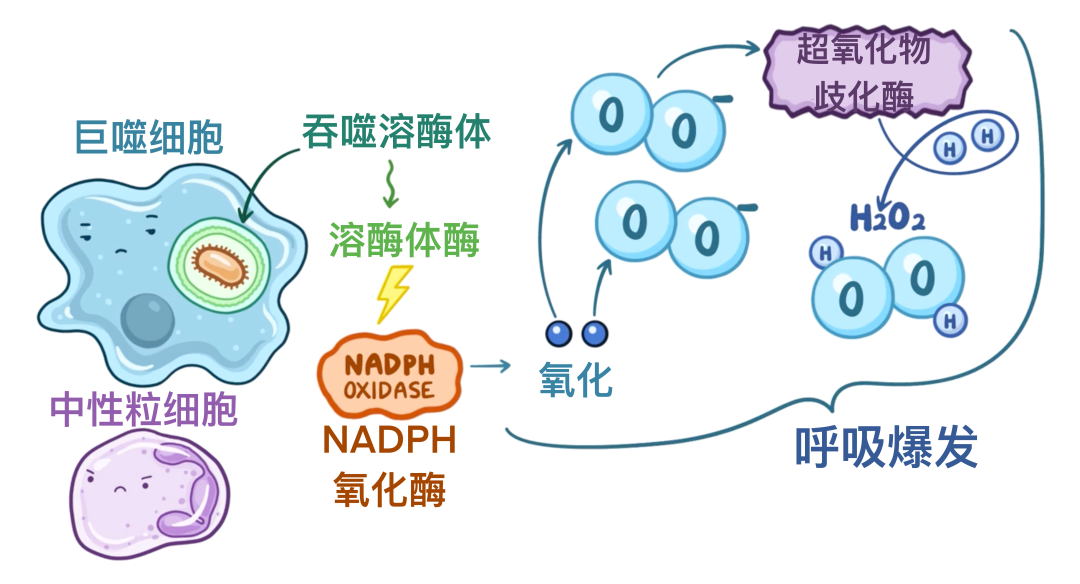
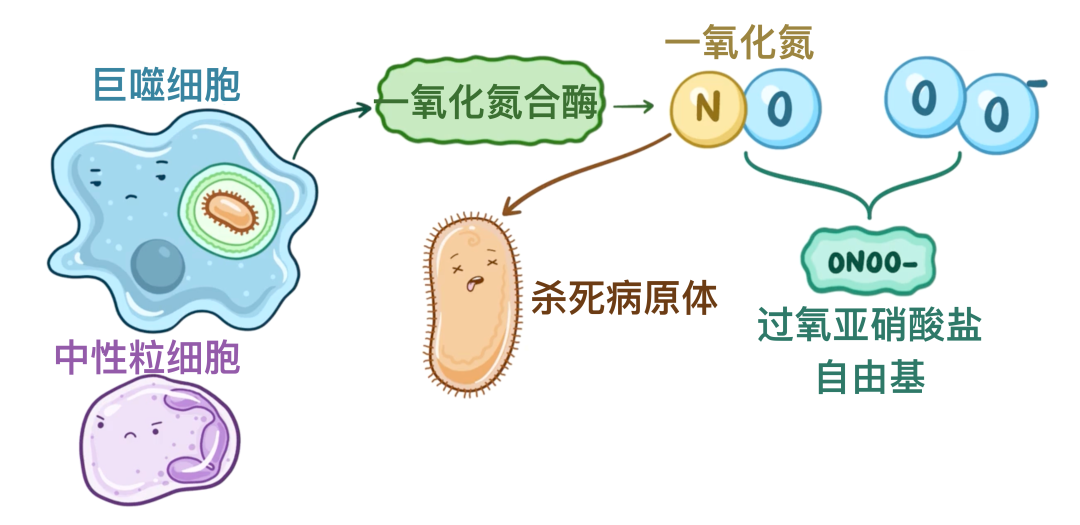
在病理状态下,自由基同样可能产生。例如炎症反应期间,巨噬细胞和中性粒细胞等吞噬细胞会生成自由基。当病原体入侵机体时,吞噬细胞会将其吞噬并形成吞噬溶酶体。
这些吞噬细胞内还含有一种名为NADPH氧化酶的酶类,当它被溶酶体酶激活后,会促使NADPH发生氧化反应并失去两个电子。此时,周围的氧分子会捕获这些电子形成超氧阴离子。
另一种称为超氧化物歧化酶的酶类,能够将这些超氧阴离子与氢离子结合生成过氧化氢。这种产生超氧阴离子和过氧化氢的过程被称为”呼吸爆发”。
此外,吞噬细胞还含有一种一氧化氮合酶,这种酶能产生具有杀菌作用的一氧化氮。整个过程中,活性氧簇与一氧化氮协同作用,共同参与对病原体的杀伤。
但一氧化氮还会与超氧阴离子发生反应,形成过氧亚硝酸自由基(ONOO—)。这些活性氧离子和分子通过破坏病原体的细胞膜结构并损伤其蛋白质来实现杀菌作用。
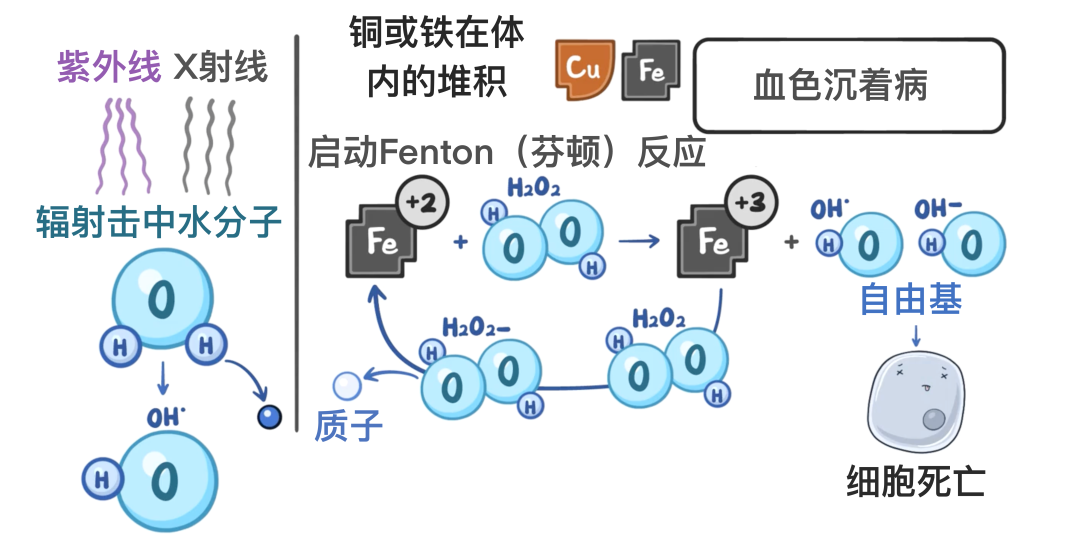
自由基产生的另一途径是暴露于电离辐射(如紫外线或X射线)。
当辐射作用于组织中的水分子时,会击出水分子中的一个电子,从而将其转化为羟自由基。
此外,当体内铜、铁等金属离子蓄积时也会诱发自由基生成。例如,血色病(hemochromatosis)就是一种因铁吸收异常增多导致的病理状态。
这些过量的铁离子会引发芬顿反应(Fenton reaction):二价铁离子(Fe²⁺)被过氧化氢氧化,生成三价铁离子(Fe³⁺)以及副产物羟自由基和氢氧根离子。随后,三价铁离子又可在过氧化氢作用下被还原为二价铁离子,同时产生过氧自由基和质子,如此循环往复,形成一个无休止的恶性循环。
长期积累的芬顿反应所产生的自由基会逐渐损害多个器官的细胞,最终导致细胞死亡并引发组织纤维化。
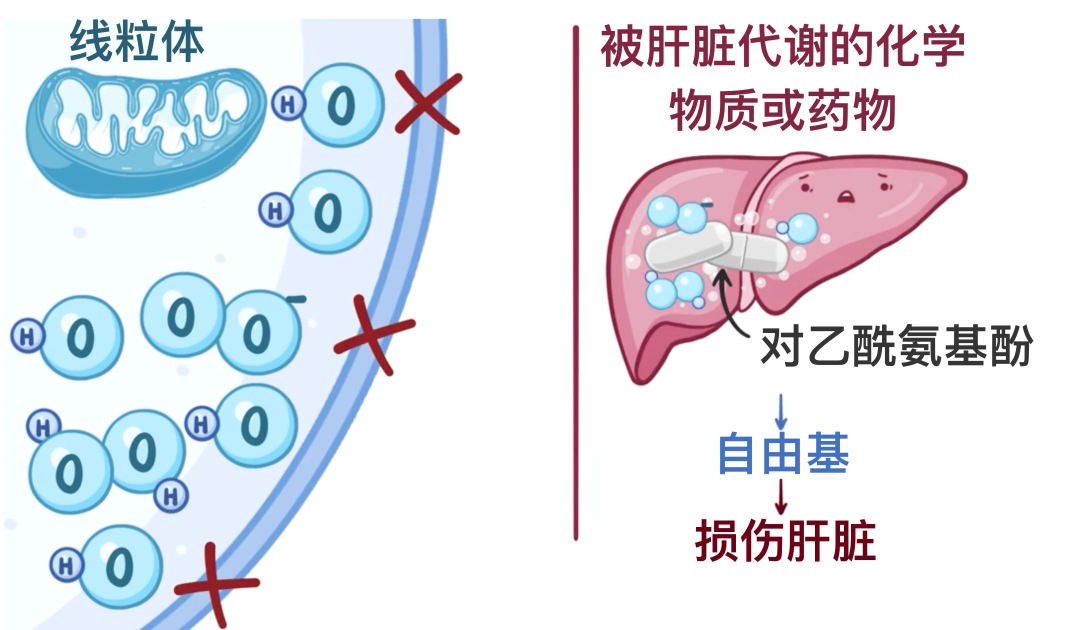
此外,当组织或器官发生缺血(血流灌注不足)时也会产生自由基。在细胞层面,缺血性损伤会促使线粒体生成活性氧簇。
若缺血组织恢复血液供应(即再灌注),反而会带入更多氧气,从而加剧氧化应激反应。然而不幸的是,这些大量涌入的氧气会与既存的自由基发生反应,进而产生更多自由基,造成更严重的细胞损伤。
这一现象称为”再灌注损伤”。最后,当外源性化学物质或药物在肝脏代谢时,也会产生自由基。例如,肝脏在分解对乙酰氨基酚(即泰诺)等药物时,会产生大量自由基,可能对肝脏造成严重损害。
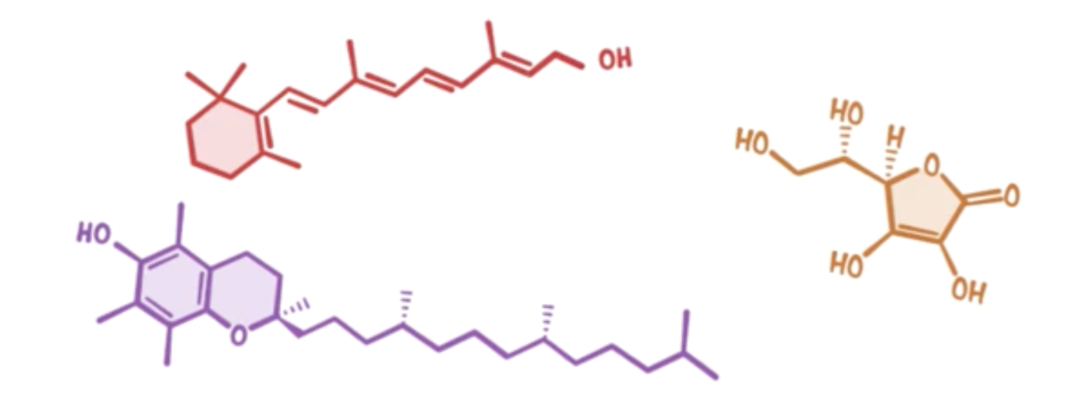
由于人体即使在正常生理状态下也会产生自由基,因此进化出了一套防御机制来调控它们。其中一种重要机制就是抗氧化剂(如维生素A、C和E),它们能够通过提供电子来中和自由基,从而保护细胞免受损伤。
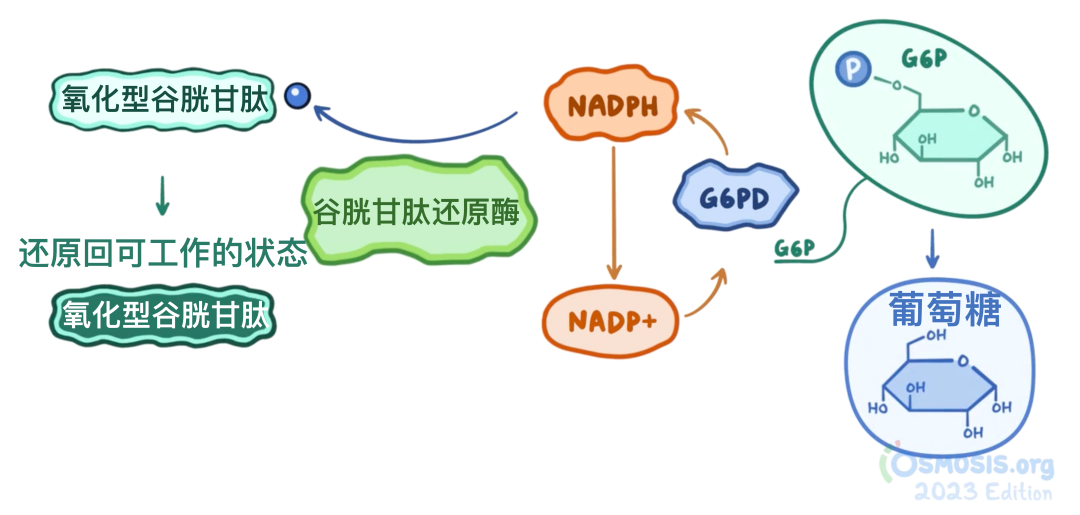
我们体内还有一种称为谷胱甘肽的分子,同样具有抗氧化作用,能够中和过氧化氢。要使这一机制发挥作用,需要两个处于还原状态的谷胱甘肽分子,它们会向过氧化氢提供一个电子和一个质子,将其转化为无害的水分子。
然而,这一过程会导致谷胱甘肽被氧化。为了让氧化的谷胱甘肽恢复功能,一种名为谷胱甘肽还原酶的酶会利用NADPH作为电子供体,将氧化的谷胱甘肽重新还原为具有活性的状态。
在此过程中,失去电子的NADPH会转变为NADP⁺。为了补充NADPH的储备,葡萄糖-6-磷酸脱氢酶(G6PD)会通过氧化葡萄糖-6-磷酸,将NADP⁺重新还原为NADPH,从而维持这一抗氧化系统的持续运作。
人体内存在多层次的自由基防御系统。葡萄糖-6-磷酸作为葡萄糖代谢产物,在非饥饿状态下可稳定供给,为NADPH再生提供底物。
金属载体蛋白通过结合金属离子发挥重要保护作用,例如转铁蛋白(transferrin)可特异性结合血液中的铁离子,铜蓝蛋白(ceruloplasmin)则负责铜离子的转运,这种结合作用能有效阻止游离金属离子参与自由基生成反应。
在酶防御系统方面,超氧化物歧化酶(SOD)能将超氧阴离子转化为过氧化氢,随后过氧化氢酶(catalase)在过氧化物酶体中将过氧化氢分解为水,而谷胱甘肽过氧化物酶(GPx)则在胞质中执行相同的解毒功能。这些酶系统共同构成了严密的自由基清除网络。
然而,当自由基的生成速率超过这些防御系统的清除能力时,氧化应激就会发生,最终导致细胞损伤。这种平衡的打破往往是多种病理过程的起点。自由基会攻击细胞膜中的脂质分子,引发脂质过氧化反应。
例如,当羟自由基攻击某个特定脂质分子时,会使其失去电子形成不稳定的脂质自由基。这个带有未配对电子的脂质自由基又会从邻近脂质分子夺取电子,从而引发连锁反应,最终导致细胞膜结构损伤。
此外,自由基还能诱导蛋白质发生氧化修饰,影响酶活性及结构蛋白功能。
在遗传物质层面,DNA的氧化损伤可能导致链断裂或诱发突变,显著增加细胞癌变风险。这种多层次的氧化损伤是自由基致病的重要分子机制。
来源网址:病理学——自由基与细胞损伤



 扫码安装网站APP(Android版)
扫码安装网站APP(Android版)


近期评论