作者:陈楚柔 黄少旭
摘要:随着教育对科技前沿的关注,关于革命性的癌症治疗方法逐渐成为命题的趋势和热点。CAR-T细胞疗法是一种革命性的癌症治疗手段,通过基因工程技术对患者自身的T细胞进行改造,使其能够识别并攻击癌细胞。涉及CAR-T细胞疗法的试题,旨在考查学生对于基因工程、免疫调节等领域知识的掌握和理解。从CAR-T细胞疗法的基本原理、发展历程、临床应用、面临的挑战及发展前景作一综述。
作者简介:黄少旭(1977—),男,硕士研究生学历,副教授,E-mail:20200611@m.scnu.edu.cn;
癌症是全球范围内的主要健康问题,传统的治疗方法如手术、放疗和化疗在某些情况下效果有限。在近年来的免疫治疗领域,CAR-T细胞疗法,正以卓越的治疗效果,成为备受瞩目的焦点。CAR-T细胞疗法是利用基因工程技术改造患者的T细胞,使其能够识别并杀死癌细胞,已在某些类型的血液癌症中取得了显著的临床效果。在高中生物学教材中,CAR-T细胞疗法的原理和应用已被纳入免疫调节部分,但由于篇幅有限,对CAR-T细胞疗法的介绍较为简略。同时,随着教育对科技前沿的关注,有关革命性的癌症治疗方法也逐渐成为命题的趋势和热点,如2024年高考江苏卷第22题就针对CAR-T细胞疗法,设计了围绕CAR-T细胞的制备过程、作用机制以及临床应用等方面的问题,旨在考查学生对基因工程、免疫调节等领域知识的掌握和理解。
1 CAR-T细胞疗法的基本原理及其发展历程
1.1 CAR-T细胞疗法的基本原理
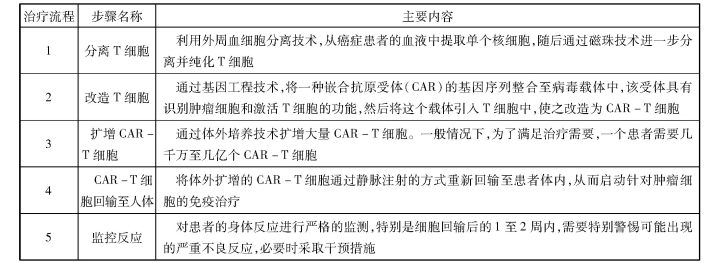
CAR-T细胞疗法的基本原理是从癌症患者血液中分离出免疫T细胞,利用基因工程技术为T细胞引入能够识别肿瘤特异性抗原的单链可变区片段(scFv)和T细胞激活信号分子,构建嵌合抗原受体。通过将这一嵌合基因片段转染到患者自身的T细胞中,使其表达嵌合抗原受体,从而赋予T细胞识别并攻击肿瘤细胞的能力。图1为CAR-T细胞疗法流程图。表1为CAR-T细胞疗法治疗流程。
图1 CAR-T细胞疗法流程图(改自D.ZC等)
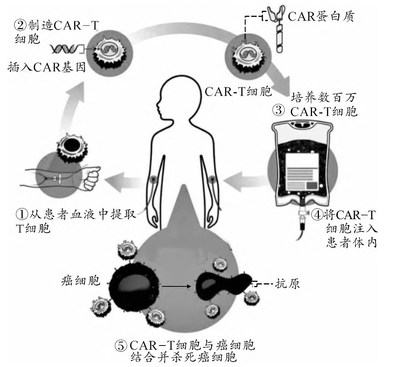
表1 CAR-T细胞疗法治疗流程
1.2 CAR-T细胞疗法的发展历程
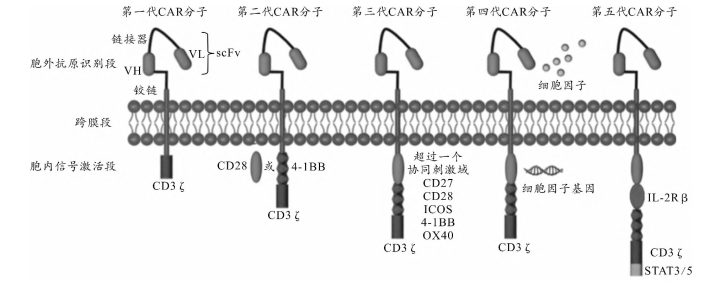
CAR-T细胞疗法自问世以来,已经经历了5代的发展。具体如图2所示。
第一代CAR-T细胞仅由能够识别特定肿瘤抗原的单链可变区(scFv)与胞内刺激信号CD3ζ直接连接而成,但由于第一代CAR-T细胞在体内的活化能力和对肿瘤细胞的杀伤效率不足,早期的临床试验并未取得预期的成功。
在第一代CAR-T细胞的基础上,在胞内区增加CD28或4-1BB等共刺激分子,研发出了第二代CAR-T细胞。目前批准上市的7款CAR-T细胞疗法产品均为第二代。
第三代CAR-T细胞在第二代的基础上,加入了第二个共刺激分子,如ICOS。
第四代CAR-T细胞则进一步加入了能够分泌细胞因子的基因,实现CAR-T细胞自分泌IL-12、IL-15、IL-18等细胞因子。
最新的第五代CAR-T细胞则在原有基础上通过增强胞内结构域中的细胞因子受体(如IL-2Rβ)和转录因子(如STAT3、STAT5),以提升CAR-T细胞的自我维持、增殖能力和激活效率。
图2第一代至第五代CAR分子的结构特征(改自潘心怡等)
2 CAR-T细胞疗法的临床应用
目前,全球市场上仅有7款CAR-T疗法产品获得批准,这些治疗方法根据它们靶向的抗原可以分为以下两类。
2.1 靶向CD19的CAR-T细胞疗法治疗血液恶性肿瘤
CD19是一种主要在B细胞表面(除浆细胞外)表达的跨膜糖蛋白,它在B细胞的发育、活化、增殖以及抗体产生等过程中起着重要作用,同时也是B细胞共刺激分子的重要部分,因此能够调节B细胞的信号传导。在血液恶性肿瘤的治疗靶点研究中,针对CD19靶点的研究是最深入的,与之相关的临床试验已超百项。目前有5种自体CAR-T细胞疗法产品可用于临床治疗血液恶性肿瘤,这些产品能够针对CD19嵌合抗原进行治疗,包括Kymriah、Yescarta、Tecartus、Breyanzi和Relma-cel。Kymriah作为首批获批的CAR-T疗法之一,积累了大量的临床研究数据,并且治疗范围广泛。Yescarta和Tecartus则是在传统抗CD19CAR-T结构上进行了优化,使得它们能够针对不同的疾病并展现出不同的治疗效果。而Breyanzi和Relma-cel作为较新的疗法,虽然临床数据尚不充分,但初步研究显示它们在提高完全缓解率或总体缓解率方面具有潜力。
2.2 靶向BCMA的CAR-T细胞疗法治疗血液恶性肿瘤
尽管以CD19靶点的CAR-T细胞疗法在B细胞恶性肿瘤的治疗上取得了显著疗效,但由于CD19在多发性骨髓瘤(MM)中的恶性浆细胞表达水平较低,因此限制了该疗法在MM治疗中的潜力和应用。因此,研究者转向寻找其他靶点,BCMA(B细胞成熟抗原)因其在多种骨髓瘤细胞系中高度表达而在其他细胞类型中几乎不表达,成为治疗MM的理想靶点。目前,Abecma和Carvykti作为两种靶向BCMA的CAR-T细胞疗法,已经获批上市。这两种疗法在治疗复发或难治性多发性骨髓瘤(r/rMM)中展现出特别的潜力,因为这些患者往往对标准治疗无效,而靶向BCMA的CAR-T细胞疗法为患者提供了新的治疗选择。
3 CAR-T细胞疗法面临的挑战与展望
虽然理论上CAR-T细胞疗法具有治疗实体瘤的潜力,但其在临床实践中的应用由于遭遇一系列的挑战而进展缓慢。尽管CAR-T细胞疗法在治疗血液恶性肿瘤方面取得了显著疗效,但其在临床应用中仍面临毒副作用和高复发率问题的挑战,这些问题不仅会削弱治疗效果,甚至在某些情况下会导致病情的进一步恶化。因此,这些问题的存在严重阻碍了CAR-T细胞疗法的推广和应用,成为亟待解决的关键问题。
3.1 CAR-T细胞疗法面临的挑战
3.1.1 毒副作用
CAR-T细胞疗法在临床上最常见的毒副作用包括细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)。CRS主要是由于CAR-T细胞识别靶细胞后释放出大量的细胞因子所引起的全身炎症反应。其临床表现包括发热、皮疹、呼吸衰竭、肝功能障碍等症状,或与循环、呼吸、泌尿和消化系统相关的症状。ICANS又称神经毒性,是一种毒性脑病状态,临床表现为神经系统损伤,如语言障碍、癫痫发作、脑水肿等,在严重情况下甚至可能导致死亡。ICANS可能与CRS同时发生,也可能独立出现。
3.1.2 高复发率
CAR-T细胞疗法治疗后的高复发率仍是一个需要进一步研究和解决的问题。CAR-T细胞疗法的高复发率部分源于肿瘤本身的特性,但更主要的是由于抗原逃逸现象。这种现象在靶向CD19的血液恶性肿瘤,尤其是B细胞急性淋巴细胞白血病(B-ALL)的临床试验中尤为常见。抗原逃逸是肿瘤细胞逃避CAR-T细胞疗法的一种机制,其中肿瘤细胞表面CD19的丢失是一个显著特征。对于CAR-T细胞而言,如果CD19这一靶点无法被识别,CAR-T细胞便无法产生免疫反应,导致失去对肿瘤的杀伤作用。这种情况下,肿瘤细胞可能会逃避免疫监视,迅速增长和扩散。因此,即便CAR-T细胞疗法在初期能够实现较高的缓解率,但患者仍有可能面临较高的复发风险。
3.2 CAR-T细胞疗法的发展前景
CAR-T细胞疗法作为一种革命性的癌症治疗方法,代表着精准医疗的前沿。首先,与传统的化疗手段不同,CAR-T细胞疗法能够精准地识别肿瘤细胞的特定抗原,从而提供更高水平的特异性和疗效。其次,相较于其他靶向治疗方法,CAR-T细胞疗法的优势在于其是通过激活患者自身的免疫防御机制对肿瘤细胞进行特异性的攻击,同时最大限度地降低对正常细胞的损害,以此提升治疗效果。然而,CAR-T细胞疗法仍需克服治疗后引发的高毒副作用及复发率的难题。为了应对这些难题,未来的研究方向可从两方面着手:一方面可通过优化CAR-T细胞的结构设计和调整临床应用策略,增强其在实际应用中的治疗效果,提高治疗的安全性、有效性和持久性。另一方面可通过研发新的靶向抗原以拓宽CAR-T细胞疗法的适用范围,使其能够更精准地识别和攻击肿瘤细胞。未来,随着临床研究的深入和科技的不断进步,CAR-T细胞疗法有望在更多类型的癌症中发挥重要作用,为患者带来新的希望。
来源:陈楚柔,黄少旭.CAR-T细胞疗法研究概述[J].中学生物教学,2025,(26):61-64.



 扫码安装网站APP(Android版)
扫码安装网站APP(Android版)


近期评论