来源公众号:草草之家 作者:黄有凯
基因工程是自主命题压轴大题。
基因工程越来越向应用方向考!
CRISPR-Cas9基因编辑技术也是高考的一个比较热的情景化材料。
今天我们就用一篇文章讲清什么叫CRISPR-Cas9基因编辑!
一、什么是基因编辑?
现在对生物性状的改造有很多发展。
比方说定向突变、基因敲除。
还有一种就是对基因进行编辑。
基因编辑是一种精准定向修改生物体基因组DNA序列的生物技术。
就像用“分子剪刀”对生命的遗传密码进行剪切、插入、替换或删除,从而改变基因的功能与表达。
它突破了传统育种的随机性。
它实现了对遗传信息的精确操控。
它在基础科研、疾病治疗、农业育种等领域都有革命性的应用潜力。
二、最常见的基因编辑工具
目前应用最广泛的基因编辑工具是 CRISPR-Cas系统。
其中以 Cas9 为代表,此外还有 Cas12a、单碱基编辑器、引导编辑器等衍生工具。
今天我们重点就讲一下CRISPR-Cas9基因编辑
三、核心工具原理
(一)基础工具:CRISPR-Cas9
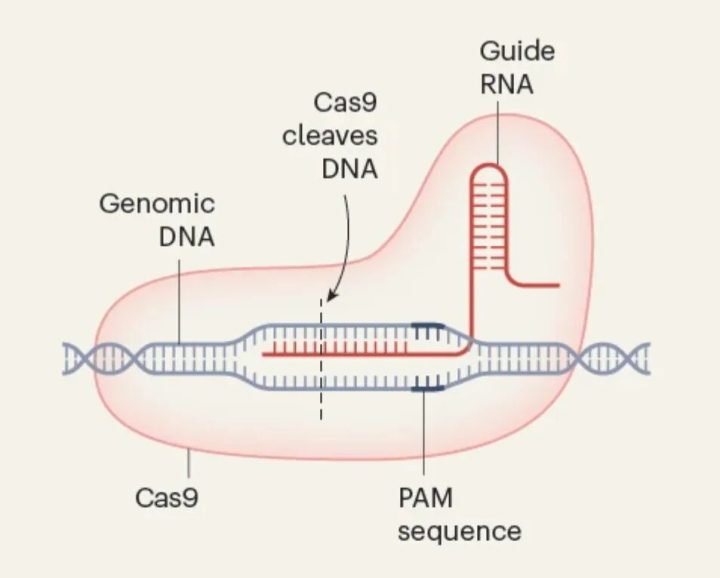
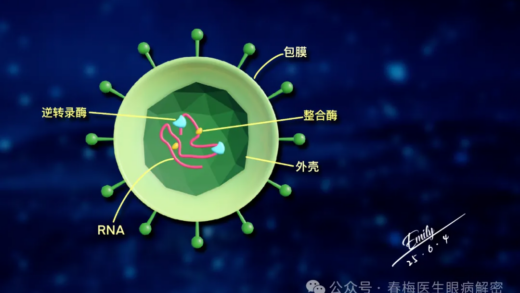
CRISPR-Cas9是一种复合蛋白质。
它的化学组分有点类似于核糖体,或者说类似于端粒酶。
里面有 蛋白质成分也RNA 成分。
其中,RNA 成分能够通过碱基互补配对的方式找到谁要切割的 DNA 序列。
然后蛋白质组分就对 DNA 序列进行切割。
下面我们结合这张图形讲它的过程。
1. 向导RNA(Guide RNA)
它像一把“精准钥匙”,通过碱基互补配对,精准识别基因组DNA(Genomic DNA)上的目标序列。
2. Cas9蛋白
像一把“分子剪刀”,在向导RNA的引导下,结合到目标DNA区域,并必须识别下游的 PAM序列(通常为NGG),才能激活其剪切活性。
3. DNA切割
Cas9在目标序列的特定位置(PAM序列上游约3个碱基处)对DNA双链进行切割,造成DNA双链断裂(DSB)。
4. 核心本质
向导RNA决定“剪哪里”,Cas9负责“动手剪”,PAM序列是Cas9识别的“身份标签”。
(二)DNA断裂后的修复机制
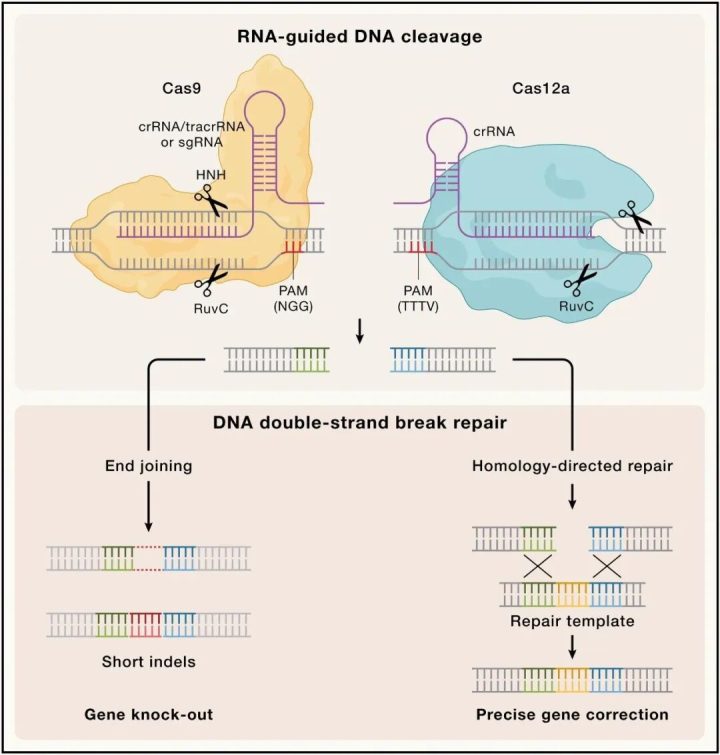
这张图分为上下两部分,完整展示了从切割到修复的全过程:
1. 上半部分:不同Cas蛋白的剪切差异
Cas9:
识别NGG型PAM序列,由HNH和RuvC两个结构域分别切割DNA的两条链,产生平末端或粘性末端。
Cas12a:
识别TTTV型PAM序列,仅由RuvC结构域完成双链切割,产生粘性末端。
2. 下半部分:两种修复途径
非同源末端连接(NHEJ)
细胞直接将断裂的DNA末端重新拼接,过程中容易产生小片段插入或缺失(Indels),导致基因移码突变,从而使基因失去功能,即基因敲除(Gene knock-out)。
这是效率最高、最常用的敲除方式。
同源定向修复(HDR)
细胞以人工提供的修复模板(Repair template)为参考,精确修复断裂位点,实现精准的基因插入、替换或修正。这种方式精度极高,但效率较低,常用于基因治疗。
(三)基因编辑技术的演进
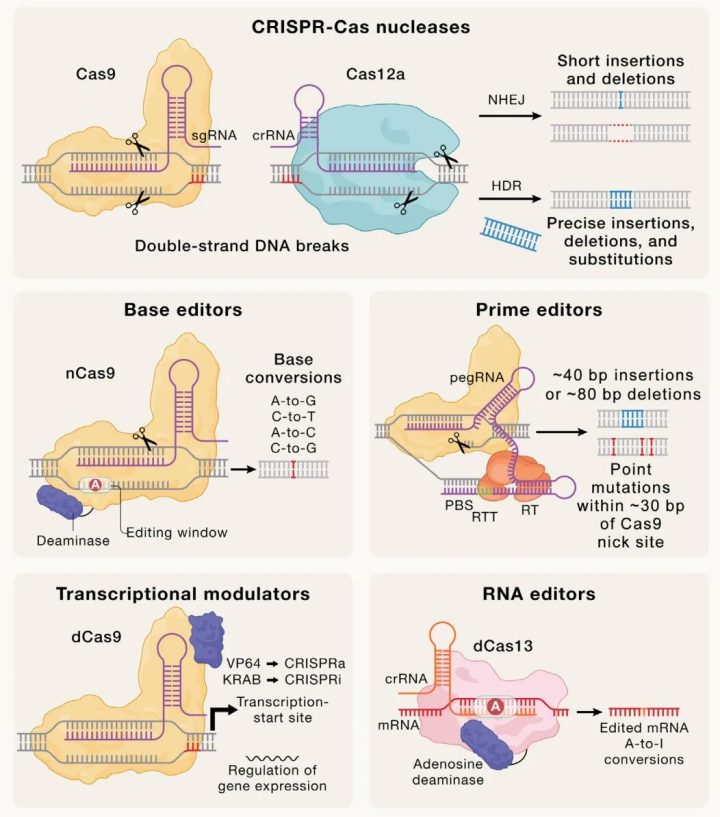
这张图展示了从经典CRISPR-Cas系统发展出的更精准的编辑工具家族:
1. CRISPR-Cas核酸酶
基础版工具,通过造成双链断裂,诱导NHEJ或HDR,实现基因敲除或大片段编辑。
2. 单碱基编辑器(Base editors)
将Cas9突变为切口酶(nCas9),只切单链,再融合脱氨酶(Deaminase),在不造成双链断裂的情况下,实现精准的单碱基转换(如A→G、C→T),避免了NHEJ的随机突变,更安全高效。
3. 引导编辑器(Prime editors)
更先进的精准编辑工具,由nCas9、逆转录酶(RT)和特殊的pegRNA引导,可实现小片段插入、删除和任意点突变,几乎能覆盖所有类型的基因修正。
4. 转录调控工具
将Cas9突变为无剪切活性的dCas9,融合转录激活/抑制结构域(如VP64、KRAB),在不改变DNA序列的前提下,激活或抑制目标基因的表达(CRISPRa/CRISPRi)。
5. RNA编辑器
以dCas13为核心,融合脱氨酶,直接编辑mRNA序列(如A→I),实现暂时性的基因功能调控,避免了对基因组的永久改变。
(四)基因编辑的实际应用
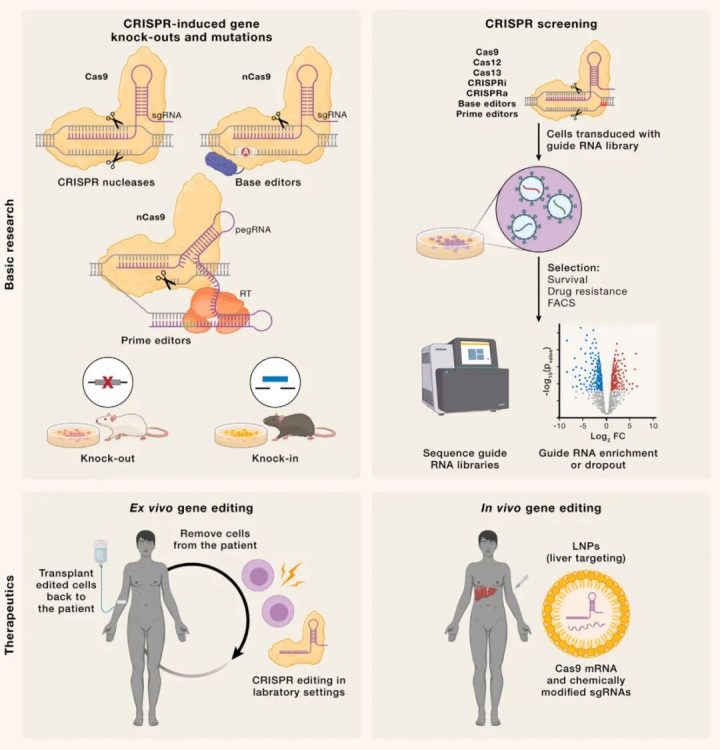
这张图从基础研究和临床治疗两个层面,展示了基因编辑的落地场景:
1. 基础研究(Basic research)
基因功能解析
通过CRISPR敲除/敲入特定基因,在细胞或模式生物(如小鼠)中观察表型变化,直接证明基因功能。
高通量筛选
构建大规模向导RNA文库,在细胞中筛选与药物抗性、癌症发生等相关的关键基因。
2. 治疗应用(Therapeutics)
离体基因编辑(Ex vivo)
从患者体内取出细胞(如造血干细胞),在实验室中完成CRISPR编辑后,再移植回患者体内。典型案例:治疗地中海贫血、构建CAR-T细胞治疗癌症。
体内基因编辑(In vivo)
通过脂质纳米颗粒(LNP)等递送载体,将Cas9 mRNA和向导RNA直接注射到患者体内(如肝脏),实现原位基因修正,为遗传病治疗提供了全新思路。
四、核心原理总结
所有CRISPR家族工具的核心逻辑都是:
1. 精准定位
向导RNA(或crRNA)通过碱基互补配对,识别目标DNA/RNA序列。
2. 效应执行
Cas蛋白(或其变体)在定位后,执行剪切、脱氨、逆转录等功能,实现对核酸序列的修改或表达调控。
3. 结果达成
通过细胞自身修复或酶促反应,最终实现基因功能的改变(敲除、激活、抑制或精准修正)。
五、CRISPR-Cas9基因编辑在高中生物基因工程大题中的常见考法及应用
1. 核心考点分类
(1)原理与组分识别
考法:直接考查向导RNA、Cas9蛋白、PAM序列的功能与作用。
例:向导RNA的作用是______;Cas9蛋白的功能类似于基因工程中的______(限制酶/DNA连接酶)。
易错点:Cas9不识别回文序列,剪切位点由向导RNA决定,区别于传统限制酶。
答题模板:
向导RNA通过碱基互补配对精准识别目标DNA序列https://wxa.wxs.qq.com/tmpl/pj/base_tmpl.html
Cas9蛋白在向导RNA引导下,识别PAM序列后切割DNA双链。
PAM序列是Cas9结合并切割DNA的必需识别信号。
(2)操作流程与技术细节
考法:写出CRISPR-Cas9基因编辑的完整步骤,或分析某一步骤的目的。
完整流程:
设计向导RNA → 构建sgRNA-Cas9表达载体 → 将载体导入受体细胞 → Cas9切割目标DNA → 细胞修复(NHEJ/HDR) → 筛选编辑成功的细胞。
例:将Cas9基因与向导RNA基因构建到同一表达载体中的目的是______。
答案:使两者在同一细胞中表达,保证向导RNA能引导Cas9精准切割目标DNA。
(3)DNA修复与编辑结果
考法:区分NHEJ与HDR的原理、结果及应用场景。
例:若要实现基因敲除,应利用______修复途径;若要精准修正突变基因,应利用______修复途径。
答案:非同源末端连接(NHEJ);同源定向修复(HDR)。
易错点:
NHEJ易产生随机Indels,导致移码突变;HDR需要提供修复模板,精度高但效率低。
(4)应用场景与对比分析
考法:结合农业育种、基因治疗等实例,分析CRISPR技术的优势。
例:与传统杂交育种相比,CRISPR-Cas9技术在作物改良中的优势是______。
答案:定向精准改造目标基因、育种周期短、可实现单基因精细操作,避免了传统育种的随机性和漫长筛选过程。
例:利用CRISPR-Cas9治疗镰刀型细胞贫血症的思路是______。
答案:设计向导RNA引导Cas9切割突变的β-珠蛋白基因,通过HDR途径将正常基因序列替换突变序列,恢复正常血红蛋白功能。
(5)安全性与伦理评价
考法:分析基因编辑的潜在风险与伦理问题。
例:CRISPR-Cas9技术可能存在的“脱靶效应”指的是______,如何降低该风险?
答案:脱靶效应指Cas9误切割与目标序列相似的非目标DNA序列;可通过优化向导RNA设计、使用高保真Cas9变体等方式降低风险。
伦理考点:生殖细胞基因编辑涉及人类遗传改变,存在伦理争议,目前仅允许在体细胞层面进行疾病治疗研究。
2. 典型大题解题思路
例题:科学家利用CRISPR-Cas9技术编辑水稻的OsBADH2基因,培育出芳香型水稻。请回答下列问题:
1. 设计向导RNA时,需要依据______的序列来确定。
2. Cas9蛋白切割DNA后,细胞通过______途径产生Indels,使OsBADH2基因失去功能,这属于______(基因敲除/基因敲入)。
3. 与传统诱变育种相比,该技术的主要优点是______。
解题思路:
1. 依据OsBADH2基因目标区域的DNA序列设计向导RNA,保证碱基互补配对。
2. 非同源末端连接(NHEJ);基因敲除。
3. 定向改造目标基因,突变效率高且可预测,避免了诱变育种的随机性和盲目性。
总之,现在的高考题都是无情景不命题。
如果我们熟悉这种情景化材料,高考的时候我们就比较容易上手。
比较节省时间,然后快速地找到解题方法。



 扫码安装网站APP(Android版)
扫码安装网站APP(Android版)

近期评论