来源公众号:北庄生物
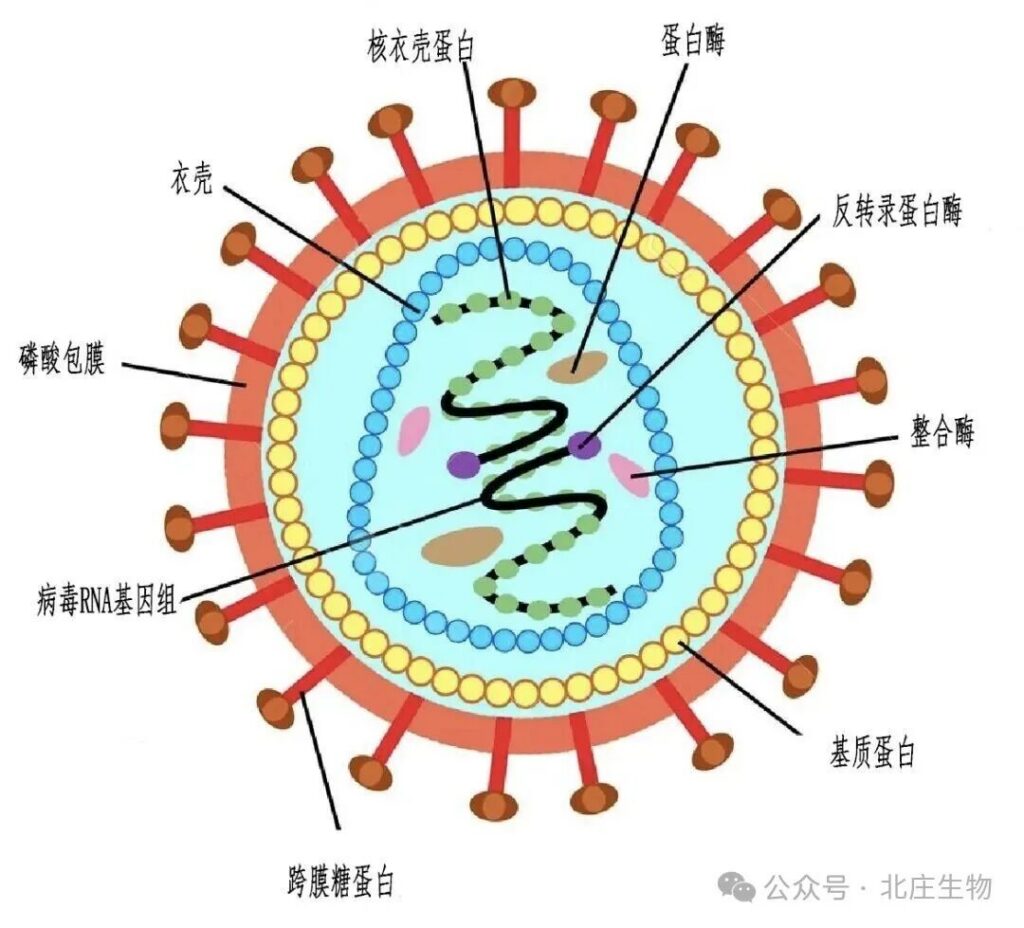
HIV(人类免疫缺陷病毒)是一种有包膜的逆转录病毒,其遗传物质是两条相同的单链RNA,并携带自身编码的逆转录酶。病毒粒子中心是由RNA和酶组成的核心,外部包裹着呈二十面体对称的蛋白质衣壳,共同构成核衣壳。最外层是来源于宿主细胞膜的脂质包膜,膜上嵌有病毒编码的糖蛋白复合物,其中gp120亚基负责识别并结合宿主细胞表面的CD4受体及趋化因子受体(如CCR5或CXCR4),gp41亚基则在结合后介导病毒包膜与细胞膜的融合,使病毒核心进入细胞。
HIV病毒的侵染过程
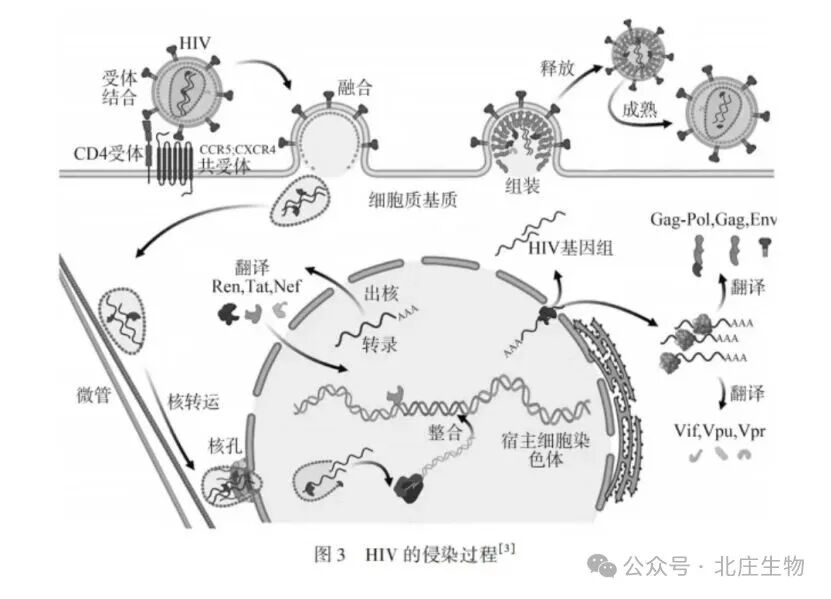
第一步:吸附与侵入
此过程发生在宿主细胞的质膜(细胞膜)。
1. 识别与吸附:HIV病毒粒子表面的包膜糖蛋白gp120,如同“钥匙”,特异性识别并结合宿主细胞(主要是CD4⁺ T细胞)质膜表面的“锁”——CD4受体蛋白。同时,病毒还需要结合细胞表面的趋化因子受体(如CCR5或CXCR4)作为共受体,才能完成高亲和力的锚定。
2. 膜融合与侵入:结合后,gp120/gp41复合体发生构象变化,暴露出内部的疏水融合肽段(gp41的一部分)。该肽段插入宿主细胞的质膜中,像“锚”一样将病毒膜与细胞膜暂时连接。随后,融合蛋白发生剧烈的重排,形成一个紧密的六螺旋束结构。这一过程释放的能量,如同“捕鼠器”的弹簧被释放,将两层脂质双层拉近并融合。最终,病毒的核衣壳(含RNA基因组和酶)被释放到宿主细胞的细胞质中。部分病毒也可能通过类似“病毒吞饮”的方式,被细胞膜内吞进入内吞体,再通过膜融合进入细胞质。
第二步:逆转录与整合
此过程跨越细胞质和细胞核。
1. 逆转录(在细胞质中进行):进入细胞质后,病毒自带的逆转录酶开始工作。它以病毒的单链RNA为模板,合成一条互补的DNA链(cDNA),形成RNA-DNA杂交体。随后,逆转录酶发挥其RNA酶H活性,降解掉RNA链,再以剩下的DNA链为模板,合成第二条DNA链。至此,在细胞质中形成了病毒的双链DNA前病毒。
2. 入核与整合(进入细胞核):新合成的双链DNA前病毒,在病毒整合酶和其他蛋白的帮助下,通过核孔复合体进入细胞核。在核内,整合酶将前病毒DNA“剪接”并插入宿主细胞的染色体DNA中,成为宿主基因组的一部分。一旦整合,病毒便进入潜伏状态,随宿主细胞DNA的复制而复制,难以被免疫系统清除。
第三步:转录与翻译
此过程在细胞核和细胞质中接力进行。
1. 转录(在细胞核中进行):当潜伏的前病毒被激活(如受细胞因子刺激),宿主细胞的RNA聚合酶Ⅱ识别病毒启动子,以前病毒DNA为模板,转录出病毒mRNA和新的病毒基因组RNA。
2. 翻译(在细胞质中进行):病毒mRNA通过核孔进入细胞质,与宿主细胞的核糖体结合,翻译合成病毒所需的各种蛋白质,包括结构蛋白(如衣壳蛋白、包膜蛋白)、酶(逆转录酶、整合酶、蛋白酶)和调节蛋白。
第四步:装配与释放
此过程主要在细胞质和细胞膜完成。
1. 装配:新合成的病毒RNA基因组和蛋白质在细胞质中运输并聚集,通常在靠近细胞膜的内侧进行装配。衣壳蛋白包裹RNA基因组形成核心,其他蛋白和酶也组装进去。
2. 出芽与成熟:装配好的病毒核心移动到细胞膜下,与嵌有病毒包膜糖蛋白(gp120/gp41)的细胞膜区域结合,以“出芽”的方式包裹一层宿主细胞膜作为自己的包膜,脱离细胞。刚出芽的病毒还不具完全感染性,需要病毒自带的蛋白酶将多聚蛋白前体切割成有功能的成熟蛋白,病毒粒子才最终成熟。
基于侵染过程的治疗方法及其依据
对上述侵染机制的深入理解,是设计抗HIV药物的根本依据。现代疗法旨在阻断病毒生命周期中的关键环节。
1. 融合/进入抑制剂:
依据:针对第一步的吸附与膜融合。
方法:如恩夫韦肽,它模拟gp41的融合肽段,竞争性结合,阻止病毒包膜与细胞膜发生有效融合。
2. 逆转录酶抑制剂:
依据:针对第二步的逆转录过程。
逆转录酶是病毒复制独有的关键酶,且错误率高(“每转录一条病毒RNA就产生一个错误”),是理想的靶点。
方法:如齐多夫定(AZT),作为核苷类似物,掺入正在合成的DNA链中,导致DNA链合成终止。
3. 整合酶抑制剂:
依据:针对第二步的整合过程,阻止前病毒DNA插入宿主基因组,从源头上阻断病毒建立永久性感染。
方法:如雷特格韦,抑制整合酶的活性。
4. 蛋白酶抑制剂:
依据:针对第四步的病毒成熟。
病毒蛋白最初以无活性的多聚蛋白形式合成,需要蛋白酶切割才能成熟。
方法:如洛匹那韦,抑制病毒蛋白酶,使新组装出的病毒粒子不成熟,无感染性。
5. 联合抗逆转录病毒疗法:
依据:鉴于HIV的高突变性,单一药物极易产生耐药性。同时使用多种作用于不同环节的药物(如上述2-4类的组合),可以极大提高遗传屏障,有效抑制病毒复制。
总结:HIV的侵染是一场对宿主细胞结构和功能的系统性劫持。从细胞膜上的受体识别开始,到利用细胞质中的原料和酶进行复制,再到潜入细胞核篡改遗传信息,最后利用细胞膜“出芽”逃离,每一步都精准地利用了细胞的特定结构。现代抗HIV治疗策略,正是基于对这些细胞生物学过程的深刻理解,通过多靶点联合用药,最大限度地抑制病毒,从而将感染转变为可控的慢性疾病。然而,由于病毒能整合潜伏并高速突变,彻底清除感染仍是巨大挑战。
最新疗法
1. EMT-Cas12a基因编辑疗法(2025年12月):外泌体搭载Cas12a“基因剪刀”,精准切割感染细胞内HIV DNA,已进入临床研究阶段。
2. Brec1重组酶疗法(2025年8月):特异性识别HIV前病毒保守序列,从宿主基因组切除病毒DNA,即将开展1b/2a期临床试验。
3. 三联组合免疫疗法(2024年4月启动临床试验,2025年12月更新数据):治疗性疫苗+广谱中和抗体+TLR9激动剂联用,激活干细胞样CD8⁺T细胞,延缓病毒反弹。
4. mRNA治疗性疫苗(2025年6月):编码HIV包膜蛋白,诱导广谱中和抗体与免疫记忆,处于1期临床试验阶段。
5. 天坛痘苗载体疫苗(2025年12月):激活特异性抗体与T细胞双重应答,已完成1期临床,2期试验推进中。
来源网址:HIV的侵染过程及其治疗依据



 扫码安装网站APP(Android版)
扫码安装网站APP(Android版)



近期评论